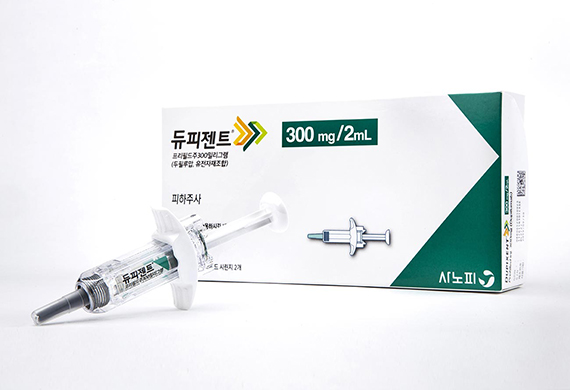
2형 염증질환 분야의 절대강자 듀피젠트(두필루맙)가 최초 수포성 유사천포창(bullous pemphigoid, BP) 치료 적응증을 확보했다.
사노피와 리제네론은 20일(현지시간) 인터루킨 4/13억제제 듀피젠트가 수포성 유사천포창 성인환자 치료를 적응증으로 FDA 승인을 받았다고 발표했다. 이번 승인으로 피부 희귀질환인 수포성 유사천포창 치료를 위한 최초이자 유일한 표적 치료제가 됐다.
승인은 LIBERTY-BP 2/3상(NCT04206553)이 기반이다. 106명의 BP환자를 대상으로 진행한 임상으로 1차 평가변수는 16주차까지 듀피젠트와 표준치료인 경구 코르티코스테로이드 병용 이후 별도의 구조요법 없이 20주 동안 듀피젠트를 단독 복용한 환자 중 재발 없이 임상적으로 질환의 개선을 보인 환자의 비율이다.
듀피젠트 투약군은 36주차에 20%가 지속적인 질병의 완화를 경험한 반면 위약군은 4%에 그쳤다. 또한 표준치료인 경구 코르티코스테로이드 복용량을 줄이면서 질병의 재발이 없는 환자의 비율은 59%대 16%, 치료 기간 동안 구조요법이 필요 없는 비율은 42%대 12%였다. 16주차까지 완전 관해와 스테로이드 중단을 달성한 비율은 38%대 27%다.
2차 평가변수인 질병의 심각도가 90% 이상 감소한 비율은 41%대 10%, 가려움증 감소는 40%대 11% 등으로 통계적 유의성을 확보했다. 이상반응의 발생 비율은 유사했으며 듀피젠트 투약군에서 더 흔한 부작용은 말초부종, 관절통, 허리통증, 시야흐림, 천식, 결막염, 변비, 상기도 감염 등이었다.
듀피젠트는 지난해 130억 7200만 유로(한화 약 20조원)의 매출을 올리며 2형 염증질환 분야에서 절대강자의 지위를 확보하고 있다. 적응증은 2017년 아토피피부염 치료제로 FDA 승인을 받은 이후 천식, 비용종 동반 만성부비동염, 호산구성 식도염, 결절성 양진, COPD, 자발성 두드러기 등에 이어 8번째다.
수포성 천포창은 고령층에서 주로 발생하는 만성 자가면역 피부질환이다. 면역체계 이상으로 피부에 물집이 형성된다. 가려움증을 동반한 수포가 손과 발, 복부, 사지에 주로 나타나며, 병의 진행 정도에 따라 전신으로 확산되기도 한다. 기존에는 고용량의 경구 스테로이드나 면역억제제 중심의 치료가 이뤄졌으나, 부작용 위험이 높아 고령 환자에게는 치료 옵션에 제약이 있었다.
후원하기





 서울 25º
습도 75%
서울 25º
습도 75% 수원 24º
습도 90%
수원 24º
습도 90% 대전 27º
습도 80%
대전 27º
습도 80% 부산 25º
습도 75%
부산 25º
습도 75%










