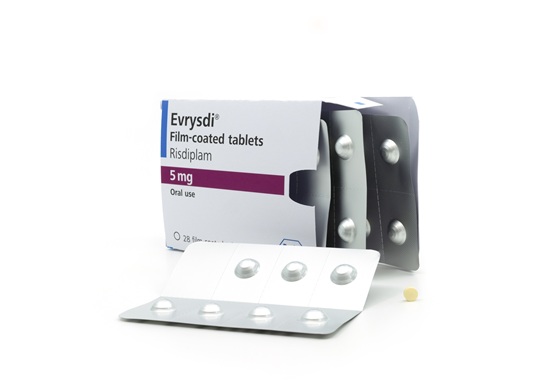
한국로슈의 척수성근위축증(SMA) 치료제 에브리스디(Evrysdi)가 기존 액상제제에 이어 정제 제형에 대해 식품의약품안전처 허가를 받았다.
식품의약품안전처는 지난 13일 에브리스디의 정제 제형(성분명 리스디플람, Risdiplam)을 허가했다. 이번 허가로 환자들은 액상과 정제 중 상황에 따라 복약 형태를 선택할 수 있게 됐다.
새롭게 승인된 정제 제형은 2세 이상, 20kg 이상 환자가 투약 대상이다. 환자는 정제를 물과 함께 삼키거나 물에 녹여 복용할 수 있다. 1일 1회 복용하며 식사와 관계없이 가능하다.
에브리스디 정제는 실온 보관이 가능해 이동과 보관이 용이하다는 점에서 복약 편의성이 향상됐다. 기존 건조시럽의 경우, 액상화한 이후 냉장보관이 필수였다.
허가는 정제와 기존 액상제제 생물학적 동등성을 입증한 임상 결과를 바탕으로 이뤄졌다. 성인 47명을 대상으로 한 연구에서 정제와 액상형은 식전·식후 상태 모두에서 생물학적으로 동등했다. 식사 여부는 약물 흡수에 영향을 주지 않는 것으로 확인됐다.
에브리스디는 SMN2 유전자의 미성숙 전령 RNA(pre-mRNA) 스플라이싱을 조절해 생존운동신경세포(SMN) 단백질의 생산을 증가시키는 기전이다. 혈관-뇌 장벽을 통과해 중추신경계를 포함한 전신에 SMN 단백질을 공급하며, 기존 임상을 통해 폭넓은 연령대에서 유효성과 안전성을 입증받았다.
한국로슈 이자트 아젬 대표는 "매일 복약이 필요한 환자와 보호자들에게 정제 제형은 일상생활에서 큰 도움을 줄 수 있는 선택지"라며 "에브리스디가 SMA 환자들의 삶의 질 향상에 기여할 수 있도록 지속 노력하겠다"고 밝혔다.
한편 SMA는 유전적 원인으로 생존운동신경세포(SMN) 단백질이 결핍돼 신경 기능이 손상되고 점차적으로 근육이 위축되는 희귀 신경근육질환이다. 신생아 약 1만 명당 1명이 발생하며, 조기 진단과 치료가 생존율과 삶의 질에 큰 영향을 미친다.
후원하기



 서울 34º
습도 55%
서울 34º
습도 55% 강릉 26º
습도 75%
강릉 26º
습도 75% 여수 30º
습도 65%
여수 30º
습도 65%










